El ciclo de la cal explica cómo la piedra caliza se transforma en cal viva y cal apagada, un proceso químico natural clave en la construcción tradicional y en el uso del mortero de cal en el arte.
El mortero de cal nace de la piedra. Todo comienza con la piedra caliza, una roca natural formada durante millones de años a partir de restos marinos. Desde el punto de vista químico, la piedra caliza es carbonato cálcico (CaCO₃).
Cuando esta piedra se somete al fuego, tiene lugar la calcinación. El carbonato cálcico (CaCO₃) se descompone, libera dióxido de carbono (CO₂) y se transforma en cal viva, u óxido de calcio (CaO).
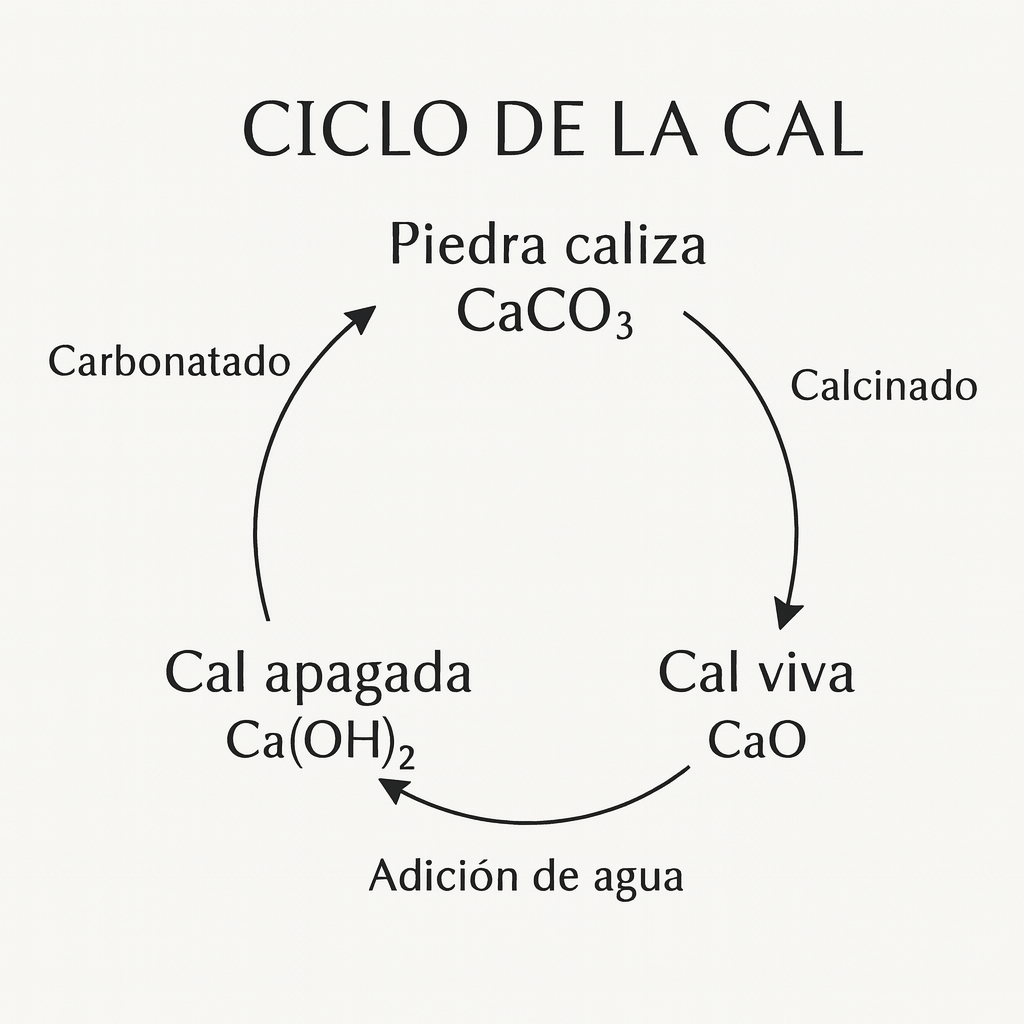
Al añadir agua, la cal viva entra en una reacción de hidratación. El óxido de calcio (CaO) se combina con el agua (H₂O) y da lugar a la cal apagada o hidróxido de calcio (Ca(OH)₂). Esta es la forma de la cal que utilizo como base del mortero en mis obras.
Una vez aplicado, el mortero inicia un proceso lento llamado carbonatación. El hidróxido de calcio (Ca(OH)₂) reacciona con el dióxido de carbono del aire (CO₂) y, con el tiempo, vuelve a transformarse en carbonato cálcico (CaCO₃). La cal se endurece y regresa a su estado mineral original.

Trabajar con mortero de cal es trabajar con un material que no se seca, sino que se transforma. Un material que respira, envejece y participa de un ciclo natural donde la química, el tiempo y la materia forman parte de la obra. Cada pieza es un fragmento de ese ciclo continuo entre la tierra, el fuego, el agua y el aire.



